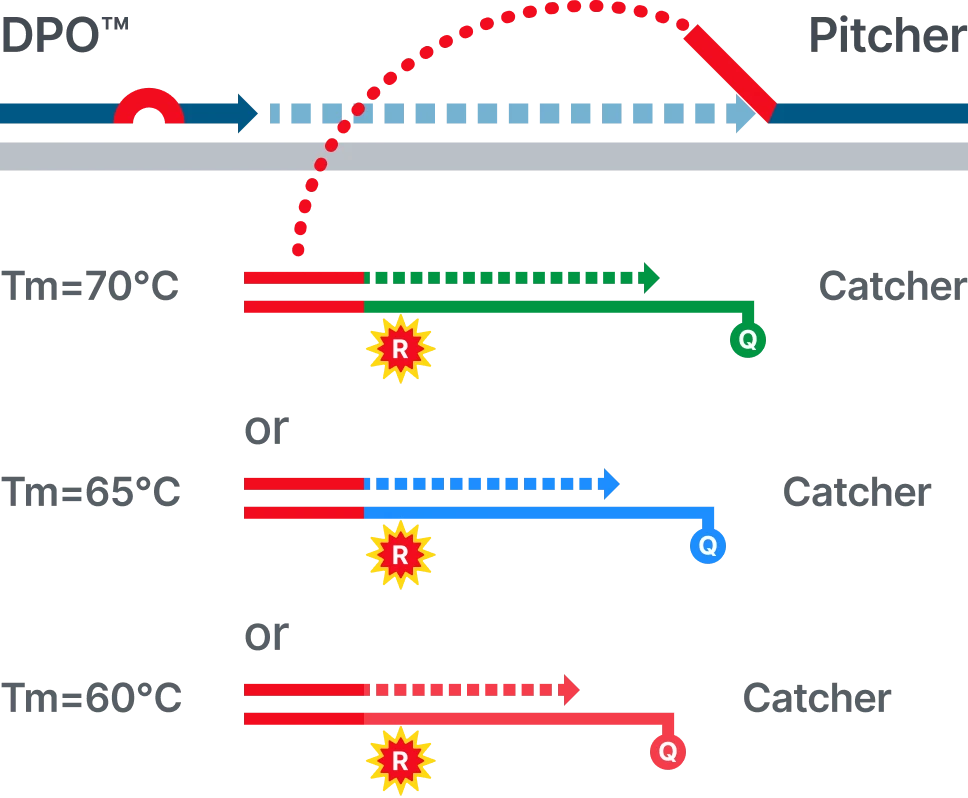
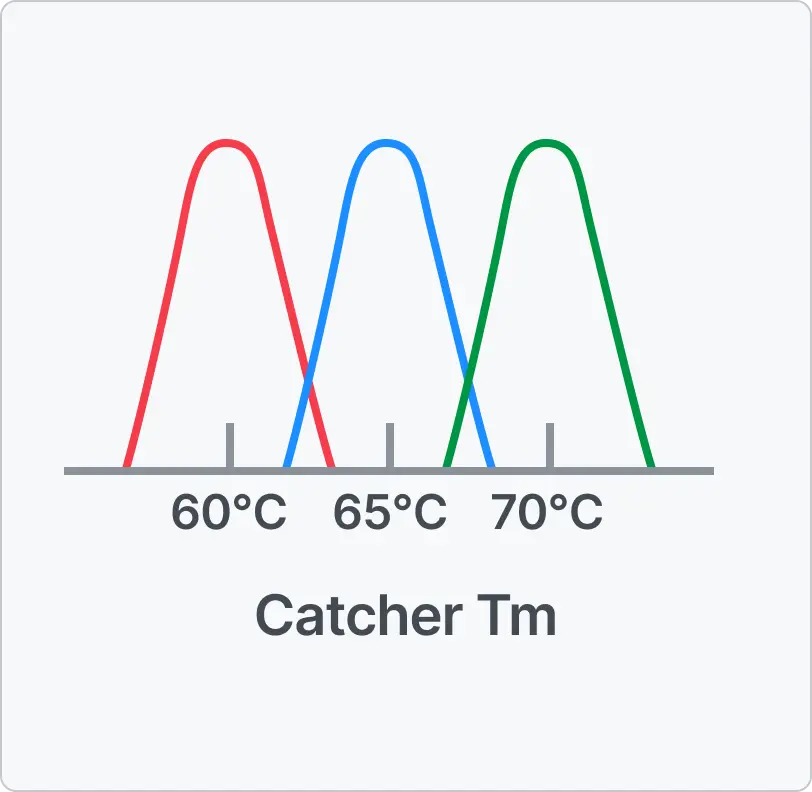
STST™는 단일 온도에서 서로 독립적이며 중첩되지 않는 형광 신호를 생성하도록 설계된 차세대 PCR 시약
플랫폼입니다. 이러한 구조적 신호 분리 방식을 통해 기존 Multiplex PCR에서 필요했던 후처리 과정을 생략하고,
하나의 채널에서 최대 5개 타겟을 정확하게 정량할 수 있습니다.
간소화된 분석 워크플로우와 직관적인 신호 해석을 기반으로 STST™는 다양한 장비 환경에서도 다중 검출 성능을
극대화하는 동시에 진단의 속도와 정확성을 향상시킵니다.
STST™ 기술 특징
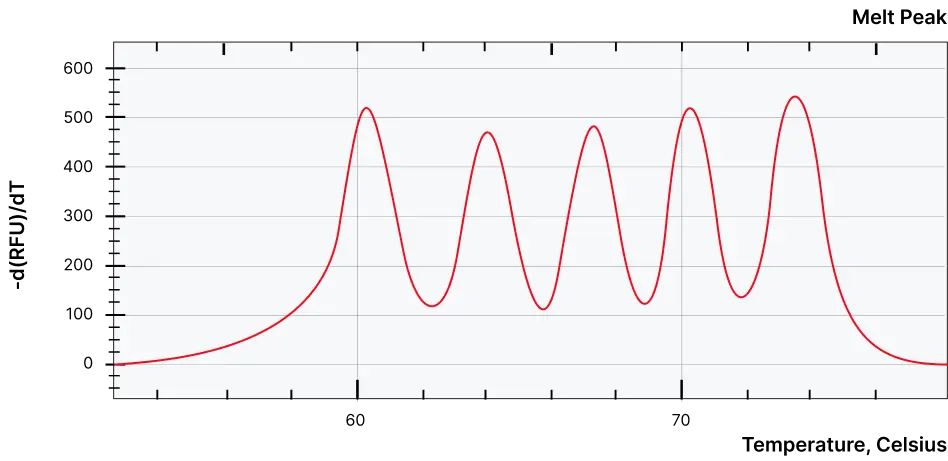
단일 채널 내 정량 가능한 다중 검출
- 하나의 채널에서 최대 5개 타겟 동시 검출
- 후처리 과정 없이 서로 독립적이며 중첩되지 않는 신호 제공
직접적이고 신뢰도 높은 신호 해석
- “보이는 그대로가 결과”인 안정적인 신호로 각 타겟을 직접 반영
- Ct 계산을 위한 추가 분석이나 신호 분리 (Deconvolution) 과정 불필요
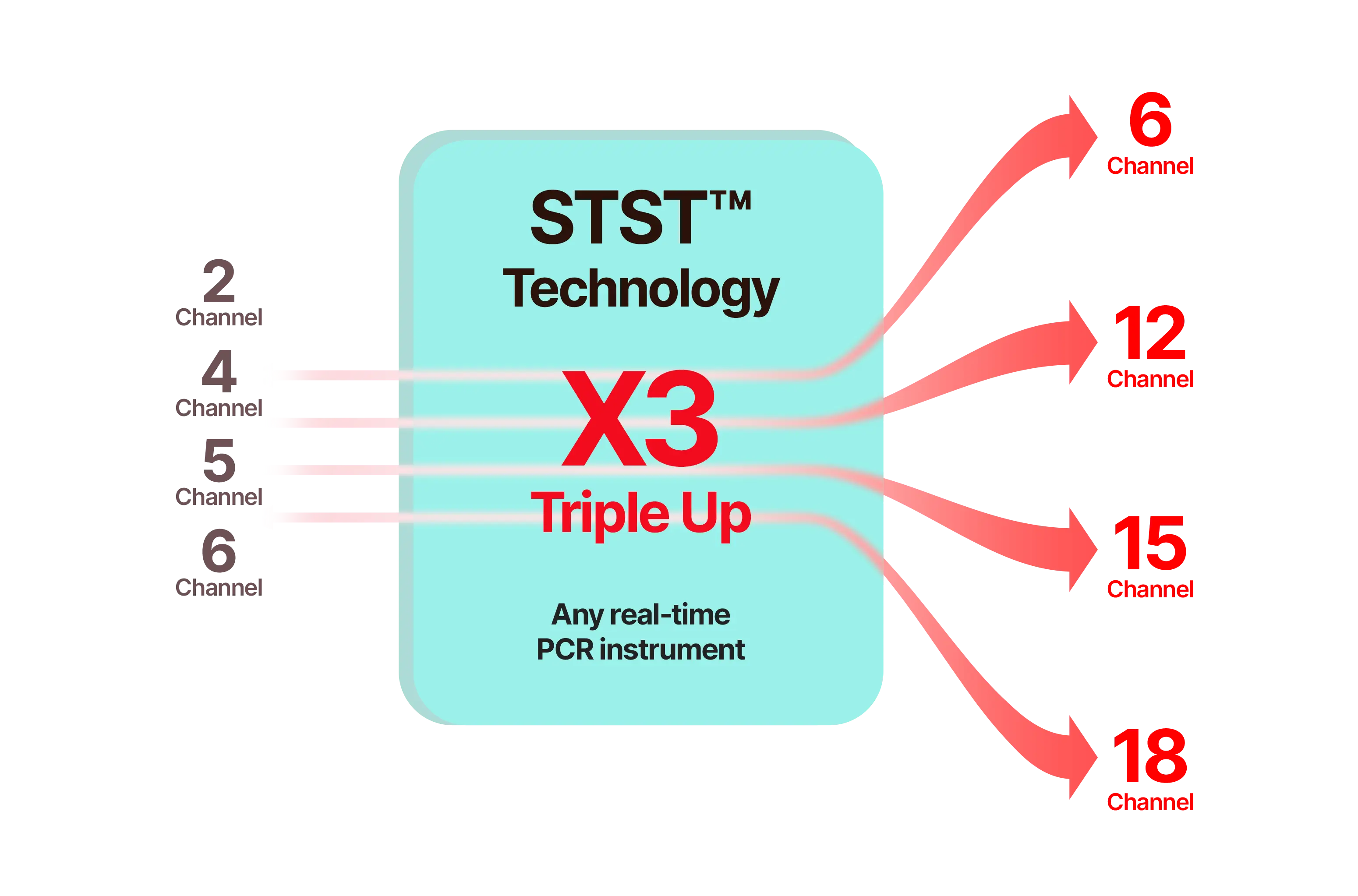
확장된 효과적인 다중 검출 성능
- 장비 하드웨어 한계를 극복한 향상된 다중 검출 성능 구현
- 단일 채널 장비에서도 다수 타겟 정량 가능
간소화된 워크플로우를 통한 신속한 의사결정
- 명확한 신호 패턴으로 빠른 결과 해석 및 보고 가능
- 분석 시간 단축을 통해 임상적 의사결정 속도 향상